医薬品分析
医薬品の元素不純物分析(ICH Q3D)
ICH Q3Dガイドラインに対応した医薬品の元素不純物評価は、2021年6月7日、第十八改正日本薬局方の一般試験法に「元素不純物」が収載されました。
今後、日本薬局方に従った元素不純物の評価・管理が始まります。
元素不純物のリスクアセスメント
元素不純物のリスクアセスメントでお困りではございませんか?
- 元素不純物試験の対象元素を絞りたい。
- 製造プラントから溶出する元素を知りたい。
- 安定性試験や過酷試験により、どのような元素が増えたか把握したい。
- 数種の中から元素不純物の少ない原薬を選びたい。

100を超える化合物の分析によるノウハウをもとに

医薬品の安全性確保のためには、元素不純物が管理閾値以上で検出された場合、混入源を特定してリスクアセスメントが必要となります。元素不純物混入の潜在的な起源は多岐にわたりますが、元素スクリーニング・元素不純物定量・オンサイト分析・溶出試験で混入経路の調査を含めたICH Q3Dガイドラインに対応した元素不純物の評価をご提案します。
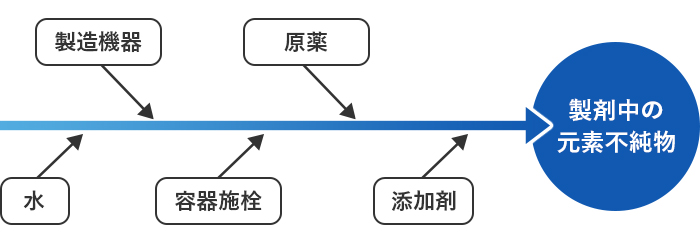
医薬品の元素不純物の評価
-
これまでの重金属試験法は、金属混在物を測定し鉛の量として表す方法で、各金属に対するリスク管理ができず元素不純物の評価としては不十分でした。
2016年に日米EU医薬品規制調和国際会議の医薬品の元素不純物ガイドライン(ICH Q3D)が日本でも発出され、元素の毒性や混入リスクに応じた24元素の許容一日曝露量(PDE)が決定されたことから、元素ごとの個別評価が始まりました。
さらに、2021年には第十八改正日本薬局方の一般試験法に「元素不純物」が収載され、医薬品の元素不純物の評価・管理ツールが日本薬局方で定められました。元素不純物の個別評価は、測定感度の高い誘導結合プラズマ質量分析法(ICP-MS)による評価に移行しています。
ICH Q3Dガイドライン評価対象元素
| 元素 | クラス | 備考 |
|---|---|---|
| As、Cd、Hg、Pb | 1 | ・ヒトに対する毒性物質 ・リスクアセスメント評価必要 |
| Co、V、Ni | 2A | ・製剤中の存在可能性大 ・すべての投与経路で評価要 |
| Ag、Au、Ir、Os、Pd、Pt、Rh、Ru、Se、Tl | 2B | ・意図的に添加された場合に評価要 |
| Li、Sb、Ba、Mo、Cu、Sn、Cr | 3 | ・比較的低毒性 ・注射剤、吸入剤で要評価 (経口剤では意図的以外評価不要) |
元素不純物試験のポイント
- 医薬品に含まれる原薬、多種類の添加剤等を分解して溶液化
- ICP-MSにより、ngレベルの極微量元素の多元素同時分析
元素不純物試験

分析ラボの特長
-
GMP(Good Manufacturing Practice)対応試験室
作業フローのOneWay化、試料間の交叉汚染防止などにより、高品質保証する 品質管理システムを構築しました。 -
クリーンルーム内にて、前処理設備と分析装置を設置
試料の分解から不純物の分析まで、クリーンルーム(清浄度: 100~10,000/ft3) 内にて実施することで、ngレベルの不純物分析を実現しています。 -
材料分析の専門家によるトータルサポート
材料分析における試料の完全分解技術を適用。 酸分解、マイクロ波分解、ふっ化水素酸分解など、適正にバリデートされた試料分解法を提案します。
その他、高薬理活性医薬品など、様々なご要望に対応しています。
-

クリーンルーム内試料調製室 -

マイクロ波試料分解装置 -

誘導結合プラズマ質量分析装置(ICP-MS)
評価の進め方
当社では、お客様の評価目的や管理基準に応じて、医薬品の金属不純物のスクリーニング、試料の分解法ならびに分析法の確立、確立した分析法バリデーション、限度試験、定量試験を提供しております。
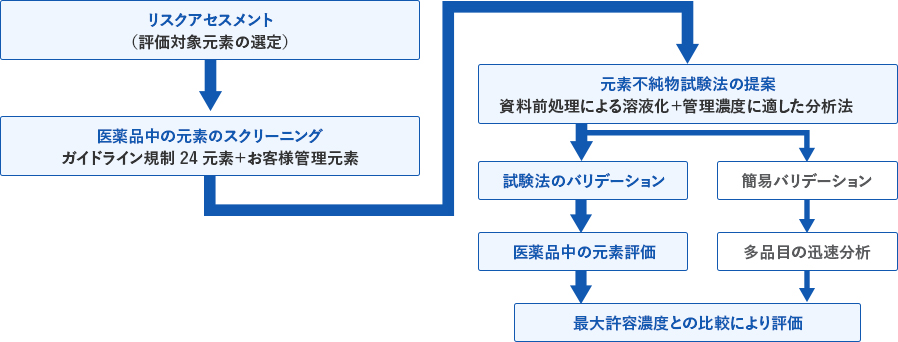
スクリーニング分析
医薬品中の元素不純物情報が不足する場合は、元素不純物試験に先立ち、1~5µg/gの濃度レベルで元素が存在するか予備的なスクリーニングを迅速かつ安価に実施します。この結果をもとに元素不純物試験法を提案し、試験法をバリデートした後に、信頼性基準またはGMP基準で元素不純物を分析します。
医薬品中の元素不純物の許容値や管理閾値との比較には、スクリーニングではなく定量分析が必要です。
スクリーニング対象元素
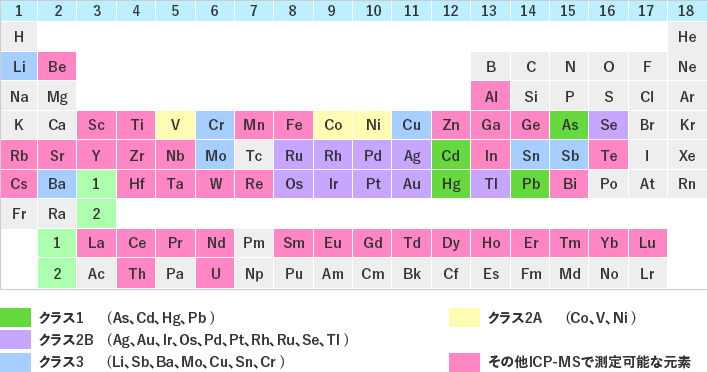
添加剤からの元素不純物分析
製剤には、原薬に加えて多種類の賦形剤や安定剤などの添加剤が混合されています。
鉱物由来の添加剤であるタルクや酸化チタンは、元素不純物の含量が高いことが知られていますが、難分解性物質であり、酸を添加するだけでは溶液化が困難です。当社は鉄鋼メーカーの分析機関ならではの前処理ノウハウにより、マイクロ波分解装置を用いることや、酸としては硝酸や塩酸だけでなく、フッ化水素酸といった酸を組み合わせることで、対象元素をロス無く完全に溶液化させて分析します。

容器からの不純物分析(E&L)
医薬品は製造、輸送、保管及び投与の過程で、包装システムの材料と化学的相互作用を生じる可能性があります。この相互作用による汚染のモニタリングは、苛酷条件で包装材料から溶出させリスクを評価する抽出物(Extractables)と実際の使用環境で溶出してくる浸出物(Leachables)を評価するため、E&L試験と呼ばれています。海外では規制が始まっていますが、日本ではまだ検討中であり、標準化された抽出条件や分析方法等の規格がありません。
当社では、医療機器分野において培ってきた溶出試験のノウハウや医薬品中の不純物分析技術をもとに、元素さらには有機物のE&L試験を海外での試験法を取り入れて提供しています。

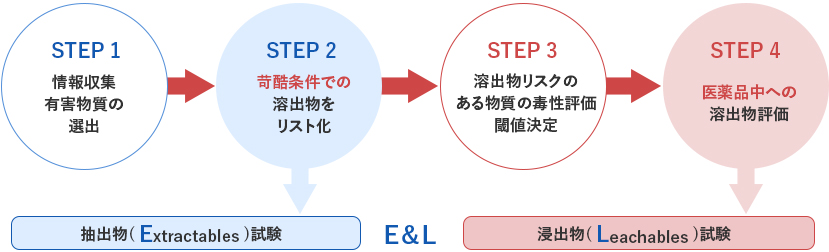
製造機器からの元素不純物分析
元素不純物の混入原因のひとつとして製造機器の構成材料が考えられます。現地オンサイトで製造機器の配管等の成分分析を行うことにより、元素不純物の混入原因のスクリーニング調査を行います。
可搬式スパーク発光装置(GREENFACT®)やハンドヘルド蛍光X線分析装置などの可搬式分析装置をオンサイトに持ち込み、サンプルを切り出さずに、その場で簡単に迅速に構成材料の成分を分析します。
オンサイト分析で原因設備を絞った後に、切り出しが可能であれば、ご指定の溶媒、使用環境の条件で溶出試験を行い、元素不純物の溶出可否を判定します。各規格に対応した試験から使用環境を模擬した試験までご要望にお応えします。
-

GREENFACT® -

ハンドヘルド蛍光X線分析装置
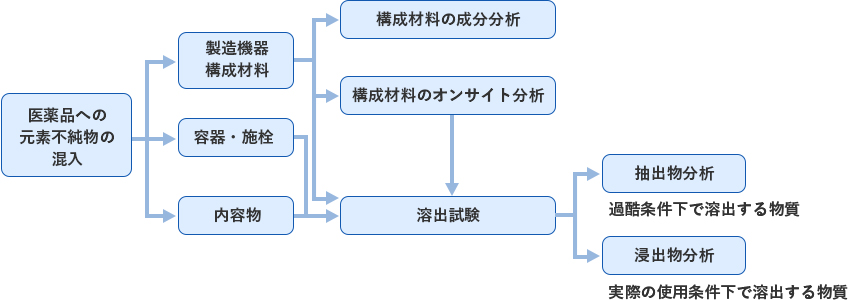
作業の流れ

関連ページ・関連リンク
- 医療・医薬品の成分分析
- 低分子医薬品不純物の構造解析・純度分析
- 化学分析
- 核酸医薬品の元素不純物分析 [事例集PDF]
- 造影剤中の元素不純物分析 [事例集PDF]
- 医薬品製造用プラスチックモジュールからの有害成分溶出(Extractables)リスク評価 [事例集PDF]
- 経皮剤のICH Q3D元素不純物分析 [事例集PDF]
- 医薬品中の残留溶媒の分析 ~ICH-Q3C対応~ [事例集PDF]
- 医薬品中の元素不純物のリスクアセスメント [事例集PDF]
- 医薬品の元素不純物分析 [事例集PDF]
- 医薬品中の元素不純物分析 [事例集PDF]
- 医薬品製造設備におけるQ3Dリスクアセスメント [事例集PDF]
- 医薬品と包装システムとの化学的相互作用 Extractables & Leachablesの評価 [事例集PDF]
- 医薬品元素不純物のスクリーニング分析 [事例集PDF]
- 医薬品の金属不純物及び残留触媒の分析(ICH Q3Dガイドライン) [事例集PDF]
- バイオ医薬品、再生医療用の培地中の不純物分析 [事例集PDF]
JFE-TEC Newsバックナンバー
- No.65(2020年10月)「新生活様式」に向けたソリューション(1)
- No.60(2019年7月)元素不純物分析(ICH Q3Dガイドライン)~日本薬局方JP17第二追補に収載日本薬局方に従って元素不純物の評価が始まります~
- No.60(2019年7月)医薬品と包装システムとの化学的相互作用(E&L)の評価技術
- No.49(2016年10月)医薬品中元素不純物分析(ICH Q3D)の紹介とJFE-TECの対応
- No.47(2016年4月)医薬品中元素不純物分析(ICH Q3D対応)
このページに関する
お問い合わせはこちらから
- JFEテクノリサーチ株式会社 営業本部
- 0120-643-777



