医薬品の品質管理
ニトロソアミン不純物分析
最高感度を持つLC/MSMSを駆使してニトロソアミン不純物の受託分析を承ります。
ニトロソアミン類とは
ニトロソアミン類とはアミン窒素上の水素がニトロソ基に置換された構造を持つ化合物の総称で、ニトロソアミン類の一部の化合物は発がん性物質であることが知られています。このことから食品/化粧品/医薬品から玩具に至るまで、幅広い分野で規制対象となっています。
特にヒトの健康に直接関わる医薬品において、製造販売事業者は、厚生労働省や米国食品医薬品局(FDA)、欧州医薬品庁(EMA)等の各国規制当局より、ニトロソアミン類が管理指標以下であることの確認また混入を低減・管理することを求められています。これらは原薬・製剤のみならず、添加剤・容器・包装材等も含めます。対象のニトロソアミン類として「医薬品におけるニトロソアミン類の混入リスクに関する自主点検」(厚生労働省)に9成分が挙げられていますが、近年では医薬品原薬そのものがニトロソ化する'ニトロソアミン原薬関連不純物(NDSRI)'が新たな問題として注目されています。
医薬品におけるニトロソアミン類分析の背景
ニトロソアミン類は国内外で、発がん性物質であるニトロソアミン類の一部医薬品への混入が判明し、自主回収となりました。
- 国内外で、発がん性物質であるニトロソアミン類の一部医薬品への混入が判明し、自主回収となりました。
- 2021年1月~ 欧州、米国にて全市場医薬品に対する調査が開始されました。
- 2021年10月 日本国内では厚生労働省より、「医薬品におけるニトロソアミン類の混入リスクに関する自主点検について」
(薬生薬審発1008 第1号, 薬生安発1008 第1号, 薬生監麻発1008 第1号)が通知され、医薬品製造販売業者に対して、9種類のニトロソアミン類混入リスクの自主点検が求められました(表1)。
なお、厚生労働省により、 「医薬品におけるニトロソアミン類の混入リスクに関する自主点検後の対応について」 (医薬薬審発0724第1号,医薬安発0724第3号,医薬監麻発0724第1号,令和7年7月24日)が通知され、ニトロソアミン類の混入リスクについては、新たな混入リスク等の知見が確認されるなど、今般の自主点検及び期限に関わらず、今後も適切に管理する必要があります。 - 当社ではGMP基準で上記9種類のニトロソアミン類分析を承ります。
| ニトロソアミン類(略号) | NDMA | NDEA | NMBA | NMPA | NIPEA | NDIPA | MeNP | NDBA | NMOR |
|---|---|---|---|---|---|---|---|---|---|
| 許容摂取量※(ng/日) | 96.0 | 26.5 | 96.0 | 34.3 | 26.5 | 26.5 | 26.5 | 26.5 | 127 |
- げっ歯類のTD50 値(腫瘍発生率が50%となる用量)等から算出。10万分の1という理論上の発がんリスクに相当する変異原性不純物の1日摂取量。
医薬品中のニトロソアミン不純物定量分析
分析事例:前処理技術を用いた試験
-
分析が困難な油脂系試料を用いた添加回収試験結果
成分 軟膏剤回収率(%) 評価基準(%) NDMA 88.7 70-130 NDEA 88.0 NMBA 72.7 NMPA 78.6 NIPEA 87.3 NDIPA 85.7 NDPA* 86.1 MeNP 78.5 NDBA 75.4 NMOR 87.3 * NDIPAの異性体
前処理技術により良好な結果が得られました。 -
クロマトグラム例

左:固相抽出なし / 右:固相抽出あり 固相抽出により、約95%の妨害成分を除去することができました。
ニトロソアミン原薬関連不純物(NDSRI)の分析
発がん性物質であるニトロソアミン類の医薬品への混入が世界的な問題となり、当局による規制が各国で実施されている中で、医薬品原薬そのものがニトロソ化する、ニトロソアミン原薬関連不純物(NDSRI)が新たな問題として注目されています。
ニトロソアミン原薬関連不純物(NDSRI)は、当局が一律に規制する成分とは異なり、分析対象が原薬成分毎に様々な形態となるため、都度試験条件の検討が必要です。
試験条件の作成~報告
当社では、GMP対応用に管理されたLC-MSを用いて、対象成分毎に試験条件の作成、バリデーション、ロット分析まで一貫して対応できます。
また、対象が不安定で定量分析が困難な場合など、ご要望に応じて高分解能MSを用いた分解物の構造解析及びその分解挙動の確認も実施できます(実施内容は、個別にお打ち合わせいたします)。事前検討、バリデーション、ロット分析の各ステップ毎に結果をご報告いたします。
試験の流れ
- ①ご依頼
- 仕様確認(対象成分・必要下限・納期など)すでに分析方法をお持ちの場合は技術移転にも対応できます。
- 対象成分の化学的特性確認(文献調査など)
- 標準試料有無の確認
- ② 事前検討(結果をご報告)
- 試料溶解の確認(溶媒選択)
- LC-MS分析条件検討
- 定量下限(定量範囲)の確認
- 再現性の確認
- ③ バリデーション(結果をご報告)
- 事前にヒアリングシートにてバリデートする項目を設定(お打ち合わせによる設定も可)
- ④ ロット分析(結果をご報告)
- バリデートした試験方法による実試験
- ⑤ ご報告
ニトロソアミン原薬関連不純物(NDSRI)の生成可否判定技術
医薬品を強制的なニトロソ化条件下で反応させ、ニトロソアミン類が生成されるか判定いたします
医薬品中の有効成分や添加剤が、ニトロソ化条件下でニトロソ化され、ニトロソアミン原薬関連不純物(NDSRI)を生成する可能性があります。
当社では、医薬品を強制的なニトロソ化条件下で反応させ、得られた生成物を分析・解析することで、ニトロソ化体の生成可否を判定し、その構造を推定いたします。
葉酸をモデル成分に用いたモデル成分での試験例
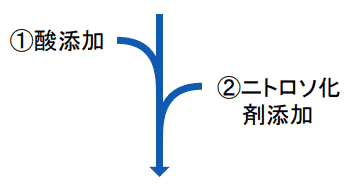
有効成分を含む溶液に酸性条件下でニトロソ化剤を添加し、強制的にニトロソ化反応を誘導します。モデル成分に葉酸(ビタミンB9)を用いた試験では、ニトロソ化体の生成を確認しました。このニトロソアミン類の生成判定は、添加剤を含む医薬品にも有効です。
また、液体クロマトグラフ/高分解能質量分析計により、生成したニトロソ化体の構造推定が可能です。
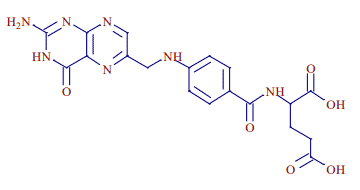
化合物名:葉酸(ビタミンB9)
分子式: C19H19N7O6
分子量: 441.4
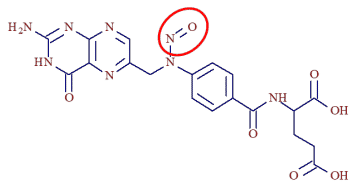
化合物名:N-ニトロソ葉酸
分子式: C19H19N8O7
分子量: 470.4
ニトロソ化された葉酸は水素(-H)がニトロソ基(-NO)に置換されるため分子量が増加(+29)いたします。
-
葉酸をニトロソ化した際のm/z 471.1370の抽出イオンクロマトグラム

ニトロソ化反応の経過を示す時系列のクロマトグラムであり、上から順に反応開始から終了までの各時点を表します。各ピークの右に示す数値は、対応するピークのシグナル強度を示します。
-
葉酸(C19H19N7O6)のニトロソ化体と推定したm/z 471.1370の
組成解析結果m/z 471.1367 推定組成式 C19H19N8O7 理論m/z 471.13712 一致度 96.2 ※ 本方法は、標準物質の合成が困難なNDSRIの評価に対して有効です。
原料及び医薬品中の亜硝酸定量分析
医薬品におけるニトロソアミン類の混入リスク評価
亜硝酸は下図に示すようにアミン類と反応して発がん性物質であるニトロソアミン生成の原因となるため、製造工程から可能な限り除去することが求められています。
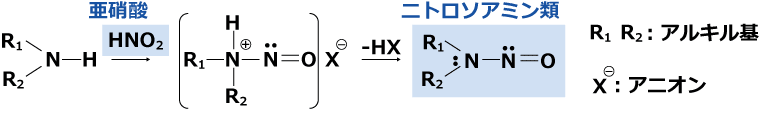
当社ではイオンクロマトグラフィーを用いた微量亜硝酸分析値の迅速なご提供によりニトロソアミン混入リスク評価をお手伝いいたします。信頼性基準にも対応しています。
微量亜硝酸分析事例
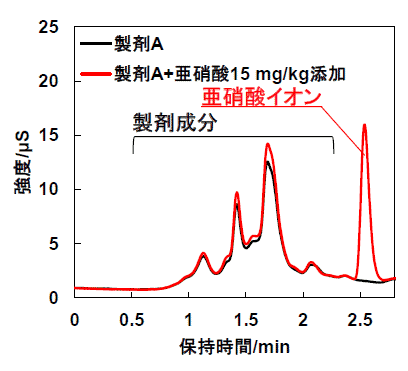
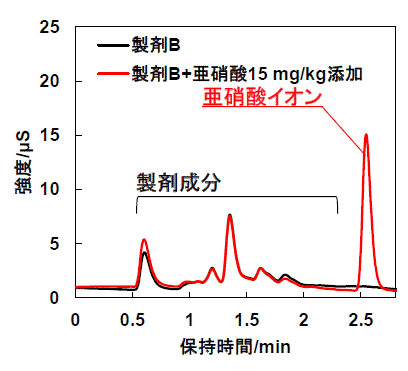
下図に2種類の製剤の分析事例を示します。各種の製剤成分から亜硝酸を分離して検出できます。また、図の事例では各製剤に含有する亜硝酸の量は1mg/kg未満であることが分かりました。
ニトロソアミン類分析装置
- 最高感度を持つLC/MSMS(タンデム型)を駆使して定量限度値0.03ppm(EMAにおけるサルタン系医薬品のニトロソアミン不純物の閾値)を実現。さらに低濃度も対応いたします(要ご相談)。
- GMP品質管理下での試験に対応いたします。
- お客様のご要望に従い、技術移転、予備検討、バリデーション試験、ロット分析様々な試験プランを提案、対応が可能です。

高分解能LC-MSでもニトロソアミン類測定の対応可能
定性分析により、規定されていないニトロソアミン原薬関連不純物(NDSRI)が原薬・製剤に含まれていないか調査することも可能です。
当社ではThermo社製LC-MS(Orbitrap)を用いた分析にも対応いたします。

関連ページ・関連リンク
- 医薬品の品質管理
- 医薬品関連情報Topics No.2(2023年10月・「ニトロソアミン類」に関する情報)
- 医薬品関連情報Topics No.1(2023年8月・「ニトロソアミン類」に関する情報)
- 医薬品中のニトロソアミン類の生成可否判定技術 [事例集PDF]
- 油脂系製剤における特定ニトロソアミン類の分析(ヘッドスペースGC/MS法) [事例集PDF]
- ニトロソアミン原薬関連不純物(NDSRI)の分析 [事例集PDF]
- 内標準法によるニトロソアミン類の定量分析 [事例集PDF]
- 原料及び医薬品中の亜硝酸定量分析~医薬品におけるニトロソアミン類の混入リスク評価~ [事例集PDF]
- 医薬品中のニトロソアミン不純物定量分析 [事例集PDF]
- ニトロソアミン類の定量分析 [事例集PDF]
- 最新鋭の装置を導入し、ニトロソアミン分析を実施しています!
JFE-TEC Newsバックナンバー
- No.81(2024年11月)化学分析の最前線 --微量成分分析--
- No.81(2024年11月)ICHガイドラインに基づく医薬品不純物分析技術
- No.75(2023年5月)【2023 年 新商品特集号】医薬品中のニトロソアミン類分析を開始しました
このページに関する
お問い合わせはこちらから
- JFEテクノリサーチ株式会社 営業総括部
- 0120-643-777